“癌症之王”总生存率近100%!潜在“best-in-class”小分子亮眼数据公布
近100%有效!FDA批准新型单抗
CSL日前宣布,美国FDA批准Andembry(garadacimab),用于预防成人和12岁及以上儿童患者遗传性血管性水肿(HAE)发作。值得一提的是,Andembry可通过自我使用的皮下自动注射器在15秒或更短时间内完成给药。此外,根据新闻稿,Andembry是用于治疗此类患者群体的首款因子XIIa靶向疗法。
HAE是一种罕见、慢性且可能危及生命的遗传性疾病,其特征是反复且不可预测的血管性水肿发作。HAE发作通常很痛苦,可能影响身体的多个部位,包括腹部、喉部、面部和四肢。HAE发生率为约每5万人中1人,任何种族群体都可能患病。通过靶向因子XIIa(一种在HAE患者肿胀发作中起关键作用的血浆蛋白),Andembry抑制HAE级联反应的顶端以防止HAE发作。
FDA的批准基于关键性安慰剂对照3期VANGUARD试验的数据支持。结果显示,62%接受Andembry治疗的患者在治疗期间未出现发作。与安慰剂相比,Andembry组患者的HAE发作次数中位减少超过99%,最小二乘均值减少89.2%;需使用按需治疗的发作中位数减少超过99%,均值减少88%;中度或重度发作的中位数同样减少超过99%,均值减少90%。试验中最常见的不良反应(发生率≥7%)为鼻咽炎和腹痛。
“癌症之王”总生存率近100%!潜在“best-in-class”小分子亮眼数据公布
Immuneering公司今日公布其在研口服、潜在“best-in-class”MEK抑制剂atebimetinib(IMM-1-104)与改良型吉西他滨/白蛋白紫杉醇方案(mGnP)联合用于胰腺癌一线治疗的2a期临床试验积极结果。在纳入的34例患者中,6个月时,联合治疗实现94%的总生存率和72%的无进展生存率,中位总生存期(OS)和无进展生存期(PFS)尚未达到。数据显示,治疗方案已展现出显著的肿瘤缩小效果,总缓解率达39%,疾病控制率达到81%。多位患者出现肿瘤持续缩小,甚至部分病灶消失。此外,该联合治疗方案也在安全性方面表现良好。
基于当前的积极数据,公司计划于2026年启动atebimetinib联合mGnP,用于胰腺癌患者一线治疗的关键性注册试验。这一进展标志着Immuneering在胰腺癌精准治疗领域的重要进步。
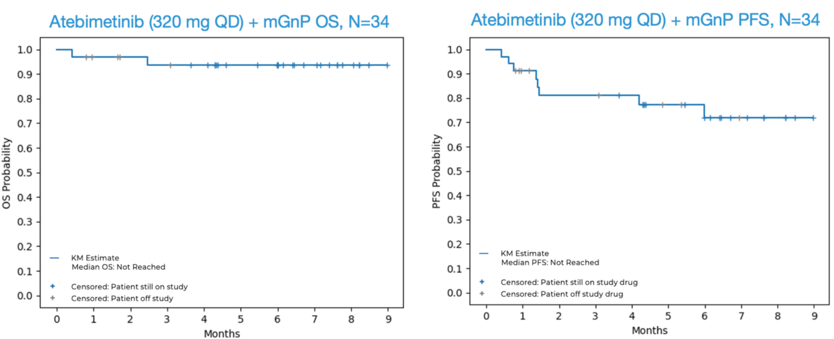
▲Atebimetinib药物试验的OS与PFS结果(图片来源:参考资料[2])
13亿美元!礼来收购Verve Therapeutics
礼来(Eli Lilly and Company)与Verve Therapeutics今日联合宣布,双方已达成最终协议,礼来将以约13亿美元总额收购Verve。此次收购将进一步强化礼来在心血管疾病领域的创新布局,特别是在基因编辑疗法方面的战略扩展。
Verve致力于开发一次给药即可能带来持久疗效的基因编辑药物,以应对动脉粥样硬化性心血管疾病(ASCVD)的根本病因。其核心项目VERVE-102为潜在“first-in-class”体内基因编辑疗法,靶向与胆固醇水平和心血管健康密切相关的PCSK9基因,适用于异合子型家族性高胆固醇血症(HeFH)及部分早发性冠心病(CAD)患者。VERVE-102目前正在开展1b期临床试验,并已获得美国FDA授予的快速通道资格。
