癌王有望终结:胰腺癌新靶点+新药联合治疗
胰腺癌素有“癌王”之称
恶性程度高、早期隐匿、治疗难度极大
长期以来5年生存率不足10%
是全球肿瘤治疗领域的“硬骨头”。
随着基础科研的深度突破与创新药企的密集布局,胰腺癌治疗迎来颠覆性变革——从KRAS靶点的“不可成药”到多款靶向药进入三期临床,从“冷肿瘤”免疫无效到双抗、细胞疗法实现长期生存,从化疗耐药到联合方案破解耐药困境,每一项进展都在改写患者的生存预期。
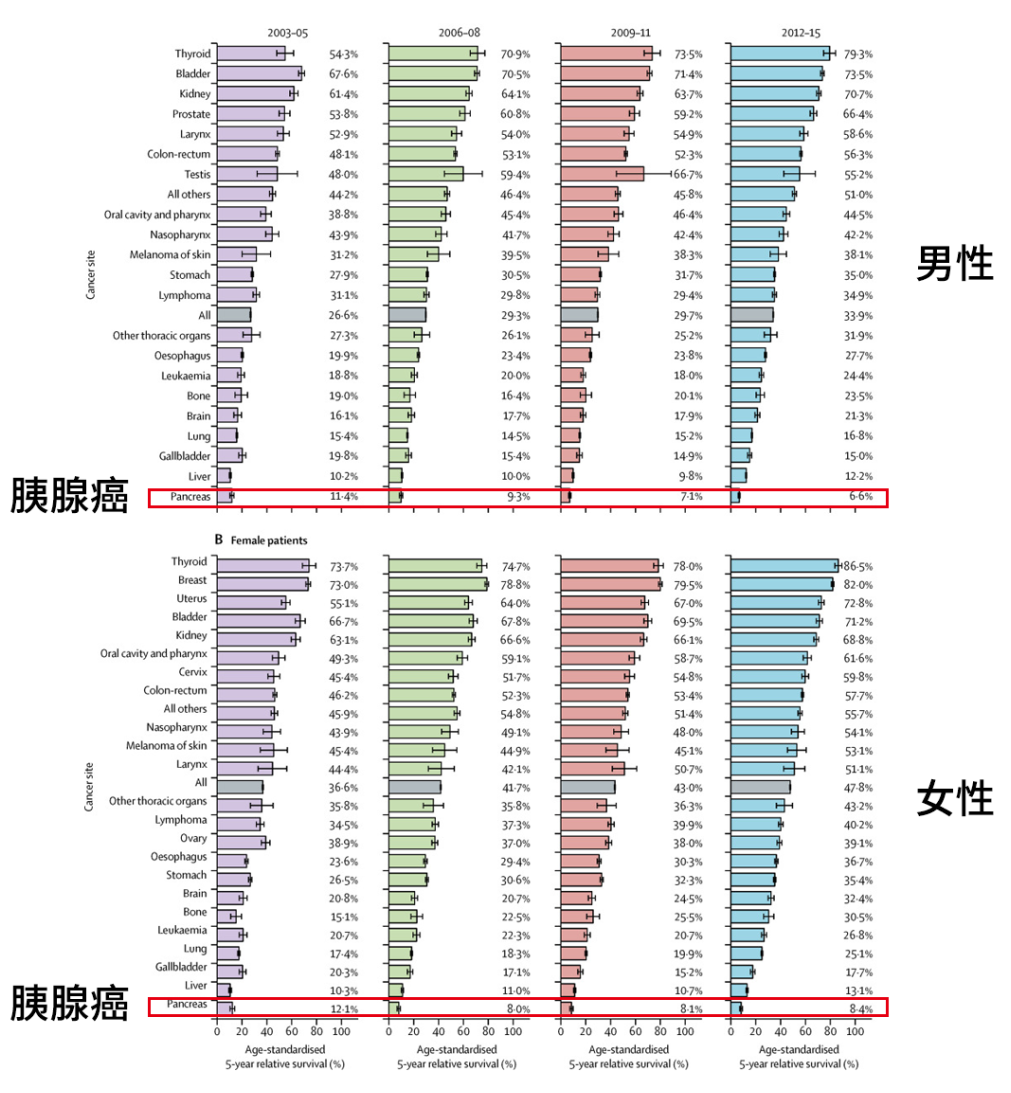
图源:参考文献[1]
靶向治疗突破:
攻克KRAS“魔咒”,覆盖主流突变亚型
KRAS突变是胰腺癌最核心的驱动基因,约95%的胰腺导管腺癌(PDAC)存在KRAS异常激活,长期以来被视为“不可成药”靶点。近几年,多项研究从机制到临床前模型实现全面突破,打破这一僵局。
1.西班牙团队三联方案清除小鼠胰腺癌,破解耐药难题
西班牙国家癌症研究中心团队在PNAS发表重磅研究,通过KRAS抑制剂+EGFR抑制剂+STAT3抑制剂的三联方案,在KRAS和TP53共突变的PDAC小鼠模型中实现肿瘤显著消退,停药后长期无复发,且副作用极低,肝肾功能、体重均无明显异常。该研究的核心突破在于同步阻断KRAS信号通路上游(EGFR)、下游及代偿逃逸通路(STAT3),从机制上减少肿瘤耐药,为人类胰腺癌的“治愈性”治疗提供了全新范式。

图源:参考文献[2]
2.中国团队构建胰腺癌类器官库,破解化疗耐药机制
中国科学院分子细胞科学卓越创新中心高栋研究组联合多家单位,在Cell Stem Cell 发布研究成果,构建了包含大量PDAC、其他亚型及正常胰腺组织的胰腺癌类器官库,通过多组学整合分析首次证实:蛋白糖基化水平升高与胆固醇代谢异常是胰腺癌化疗耐药的核心标志。团队进一步发现,化疗耐药患者联合阿托伐他汀后,部分患者肿瘤标志物下降、肿瘤缩小,为耐药患者提供了“老药新用”的全新策略。
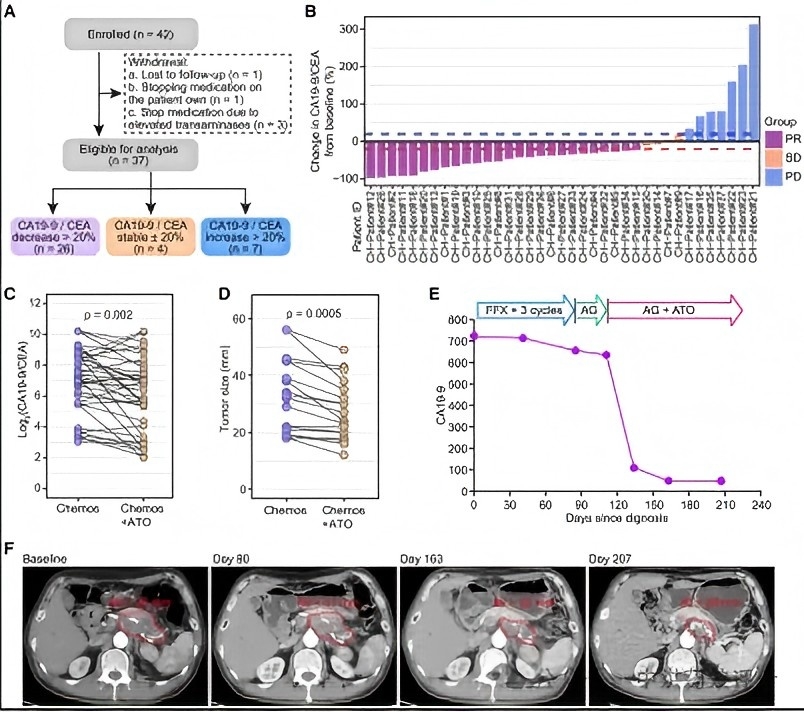
图源:参考文献[3]
3.靶向肿瘤基质,破解药物递送难题+揭示上皮-间质调控新机制
在肿瘤微环境的细胞通讯机制研究中,我国科研团队取得重大突破——中山七院张常华团队联合英国癌症研究院Axel Behrens院士团队,于2025年9月在国际顶级期刊《Nature》发表胰腺癌重磅研究,首次揭示了胰腺癌上皮-间质细胞的双向调控奥秘。

图源:参考文献[4]
企业管线布局:
上市药物扩容,临床阶段新药密集突破
(一)已上市药物:精准分层,成为标准治疗基石
药物名称 | 适应症 | 核心价值 |
卡博替尼(Cabozantinib) | 胰腺神经内分泌肿瘤(PNETs) | 填补胰腺神经内分泌肿瘤靶向治疗空白 |
奥拉帕利(Olaparib) | 胚系BRCA1/2突变的转移性胰腺癌 | 开启胰腺癌精准维持治疗时代 |
NALIRIFOX方案(脂质体伊立替康+5-FU/LV+奥沙利铂) | 转移性胰腺导管腺癌 | 目前证据等级最高的标准化疗方案 |
尼妥珠单抗 | KRAS野生型胰腺癌(联合吉西他滨) | 为KRAS野生型患者提供高性价比治疗选择 |
(二)临床阶段新药:靶向、免疫、联合方案全面开花,生存数据大幅提升
1.KRAS靶向药:从“单靶点”到“泛突变”,覆盖35%-95%患者
药物 | 研发企业 | 适应症 | 临床阶段 |
HRS-4642 | 恒瑞医药 | KRAS G12D突变晚期/转移性胰腺癌 | III期 |
RMC-6236 | Revolution Medicines | 泛KRAS突变(G12D/G12R/G12V等)转移性胰腺癌 | III期 |
INCB161734 | Incyte | KRAS G12D突变晚期PDAC | I/II期 |
Atebimetinib | Immuneering | MAPK通路激活(KRAS突变)晚期PDAC | IIa期 |
2. 免疫与双抗药物:突破“冷肿瘤”困境,联合化疗疗效翻倍
*CLDN18.2/CD47双抗:II期临床联合GnP化疗,DCR达90%以上,中位OS显著优于单纯化疗,是全球进展较快的实体瘤CD47靶向药物。
*TQB2868:正大天晴研发,PD-1/TGF-β双抗,联合安罗替尼+AG化疗,II期数据展现出优异的抗肿瘤活性,ORR、DCR及PFS率均优于传统方案,已启动III期临床,有望成为“免疫+靶向+化疗”整合方案标杆。
*索凡替尼+卡瑞利珠单抗+AG方案:和黄医药研发,II期研究中位PFS、ORR均显著优于单纯AG方案,疾病进展风险明显降低,III期临床正在推进。
3. 其他创新疗法:ADC、泛癌种靶点药物拓展适应症
*德曲妥珠单抗(T-DXd):靶向HER2的ADC药物,II期研究中,HER2高表达(IHC 3+)胰腺癌患者ORR、PFS及OS均展现出良好获益,为HER2阳性胰腺癌推荐方案。
*拉罗替尼(Larotrectinib):拜耳研发,NTRK融合抑制剂,对NTRK融合阳性胰腺癌患者疗效显著,为罕见突变患者提供精准选择。
参考文献
[1] Zeng H, Chen W, Zheng R, et al. Changing cancer survival in China during 2003-15: a pooled analysis of 17 population-based cancer registries. Lancet Glob Health. 2018;6(5):e555-e567. doi:10.1016/S2214-109X(18)30127-X
[2] Liaki V, Barrambana S, Kostopoulou M, et al. A targeted combination therapy achieves effective pancreatic cancer regression and prevents tumor resistance. Proc Natl Acad Sci U S A. 2025;122(49):e2523039122. doi:10.1073/pnas.2523039122
[3] Li Y, Tang S, Wang H, et al. A pancreatic cancer organoid biobank links multi-omics signatures to therapeutic response and clinical evaluation of statin combination therapy. Cell Stem Cell. 2025;32(9):1369-1389.e14. doi:10.1016/j.stem.2025.07.008
[4] Li H, Lan L, Chen H, et al. SPP1 is required for maintaining mesenchymal cell fate in pancreatic cancer. Nature. 2025;648(8092):203-209. doi:10.1038/s41586-025-09574-y
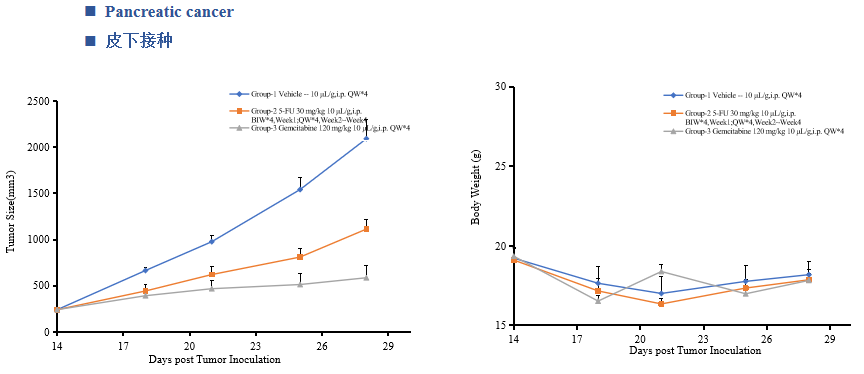
中洪博元——胰腺癌模型
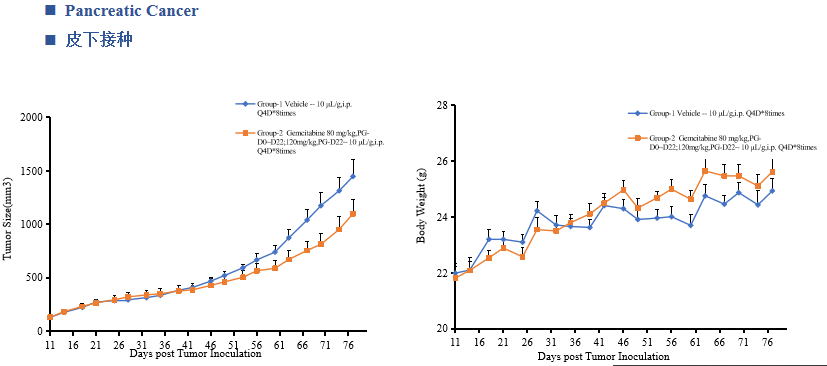
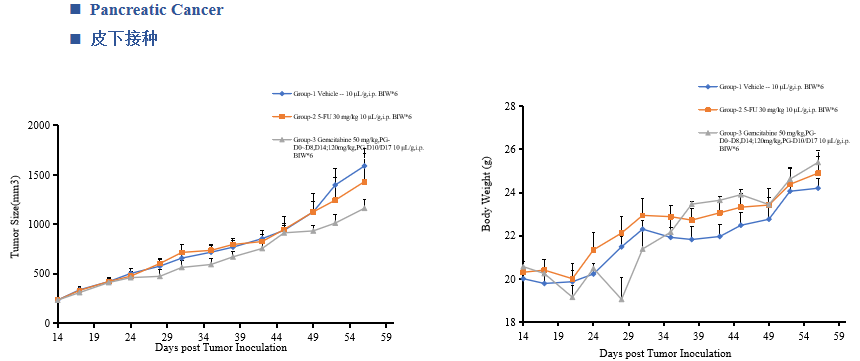
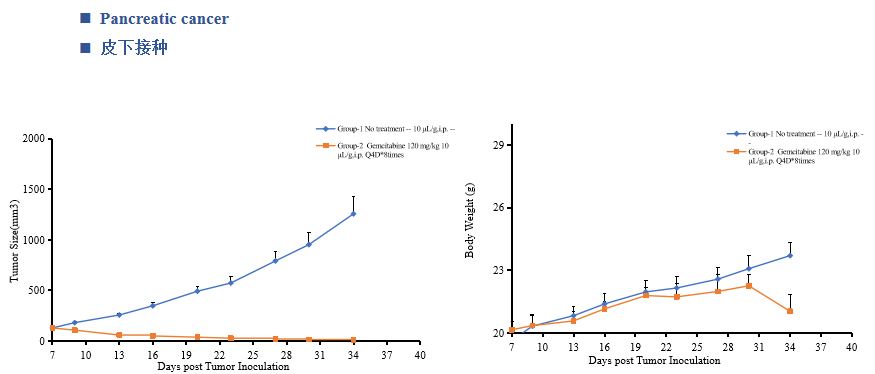
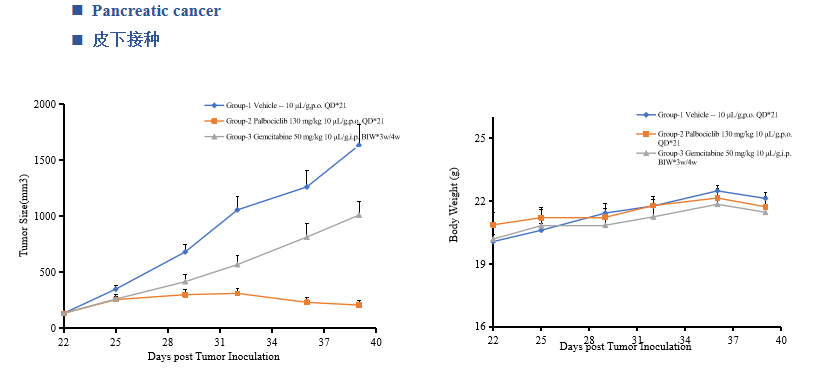
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。