科学战“压”:2025 高血压新药研发爆新进展,这些靶点成突破口
高血压作为全球最常见的慢性疾病之一,其影响范围广泛且深远。根据世界卫生组织发布的最新报告,全球约有14亿成年人患有高血压,其中近半数患者未得到有效诊断或控制,甚至不知道自己患有高血压,因为大多数患者感觉不到任何症状,这也就导致高血压成为过早死亡的一个主要原因。
图源:unsplash
从1990年的6.5亿到2024年的14亿,高血压患者激增近1倍,新增人群主要集中在低收入和中等收入国家,核心原因是老年人口数量攀升。而这一趋势,在我国同样尤为明显。高血压的普遍性与控制不足的现状,持续对全球公共卫生构成严峻挑战,也驱动着药物研发不断寻求更安全、精准的治疗方案。
目前对于高血压疾病治疗的研究,ACE、AT1R×VDCCs、NCC靶点是目前的三大研究热点。
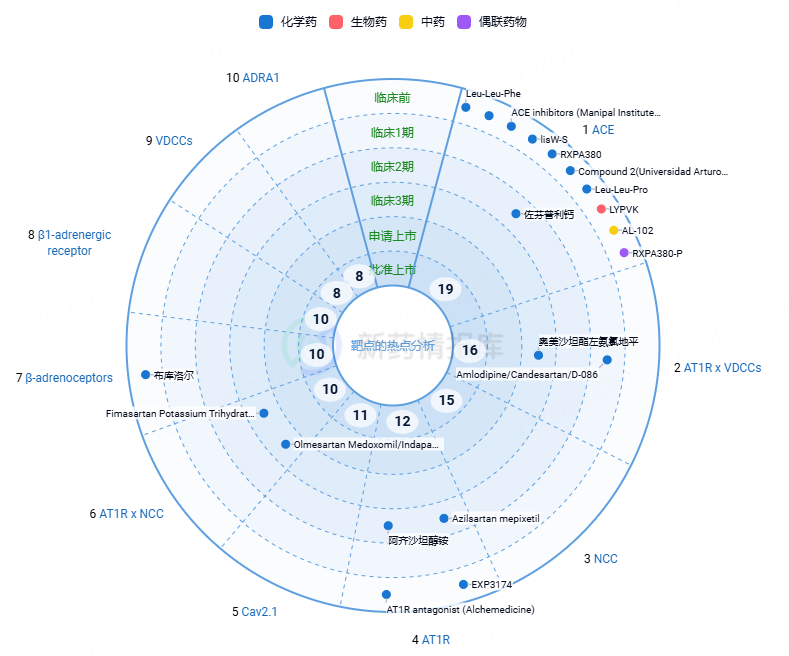
图源:新药情报库
血管紧张素Ⅰ转换酶(ACE)是一种关键的锌金属肽酶,它通过将血管紧张素Ⅰ转化为具有强烈缩血管活性的血管紧张素Ⅱ,在血压调控中发挥核心作用。目前,以ACE为靶点的药物主要分为抑制剂和调节剂两类,通过干预这一转化过程来降低血压。
1型血管紧张素受体(AT1R)是血管紧张素Ⅱ发挥作用的主要媒介。当血管紧张素Ⅱ与AT1R结合后,会引发血管收缩、血压升高、心肌肥大和醛固酮分泌等一系列反应,这些反应共同维持着基础血压与心血管功能。一种创新的联合靶向策略,通过同时拮抗AT1R并阻滞电压门控钙通道(VDCCs)的钙离子内流,能更全面地干预升压通路,从而发挥协同降压作用。
在肾脏中,钠氯协同转运蛋白(NCC)负责远曲小管中约5%-10%的钠、氯离子重吸收,对体液和电解质平衡至关重要。靶向NCC的药物通过精确抑制其功能,促进钠盐排泄,为降压治疗提供了直接作用于肾脏排钠机制的新途径。
在体内精密的血压调节系统中,这三个关键靶点如同“控制阀门”。ACE是位于上游的“核心制造厂”,负责生产强效的收缩信号——血管紧张素II,相关抑制剂通过从源头限产来实现降压。1型血管紧张素受体是这些信号的“核心接收开关”,新型联合靶向药物不仅阻断此开关,还同步抑制与之协同的电压门控钙通道,实现双重精准拦截。而NCC则像肾脏中的一个“微调水阀”,控制着水钠的重吸收,其抑制剂通过适当排水排盐来减轻系统总压力。
这三种分别针对“生产、接收、调节”环节的靶向策略,共同构成了现代降压治疗精密调控的基石。
好消息来自国内科研团队!
2025年6月16日,华东师范大学李洪林、李诗良教授团队,联合华东理工大学王蕊教授团队,在国际顶级心血管期刊Circulation(影响因子超 30)在线发表重磅研究“Inactivation of RhoA for Hypertension Treatment Through the TRPV4-RhoA-RhoGDI1 Axis”——他们找到了高血压治疗的全新靶点!研究揭示了一种针对TRPV4–RhoA–RhoGDI1轴的新型RhoA信号抑制模式,为未来降压药物开发提供了新见解,并提出了针对挑战性Rho GTP酶的创新策略。

图源:Circulation
今日国内药企的临床管线传来捷报!
据药物临床试验登记与信息公示平台数据显示,深圳信立泰药业股份有限公司连续出品两款高血压药物目前处于临床阶段,2025年12月15日公示的处于临床Ⅰ期的ETA靶点药物CTR20254965以及2025年11月25日公示的处于临床Ⅱ期Aldosterone靶点药物CTR20254965。
高血压的治疗范式正在悄然革新。从传统靶点的深耕优化,到全新信号通路的发现,再到双靶点药物、新靶向药接连进入临床——这些进展共同指向一个更精准、更个体化的治疗未来。科研的突破正转化为实实在在的临床潜力,为长期管理高血压、降低心脑血管风险提供新思路。尽管新药之路仍需时间验证,但无疑这些探索在攻克高血压又向前迈出了关键一步。
中洪博元高血压模型
1.SHR自发遗传性高血压模型
造模:10周龄雄性SHR大鼠作为模型组,WKY大鼠作为对照组,均适应性饲养1周后,再饲养8周后进行血压测量观察大鼠血压是否造模成功
造模周期:8周
治疗周期:8周
阳性药物:坎地沙坦酯、依叶片(EFA);通心络(TXL)
模型数据
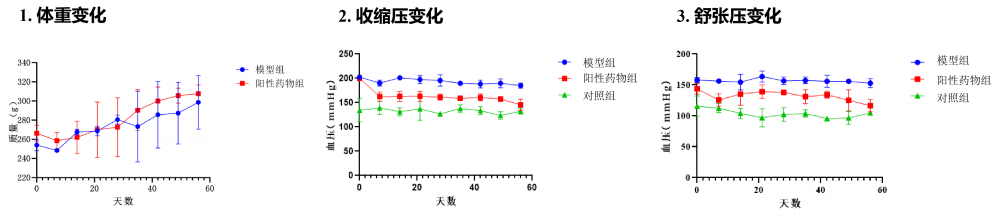
2.单肾切除+DOCA+高盐饮水构建SD大鼠继发性高血压模型
造模:SPF级SD大鼠适应性饲养1周结束后开始造模。对照组不做任何处理,模型组动物于D1进行左肾切除手术,模型组动物皮下注射DOCA(橄榄油配制),每周注射,同时NaCl饮水饲喂。
造模周期:10周
治疗周期:4周
阳性药物:缬沙坦氯氨地平片
模型数据:
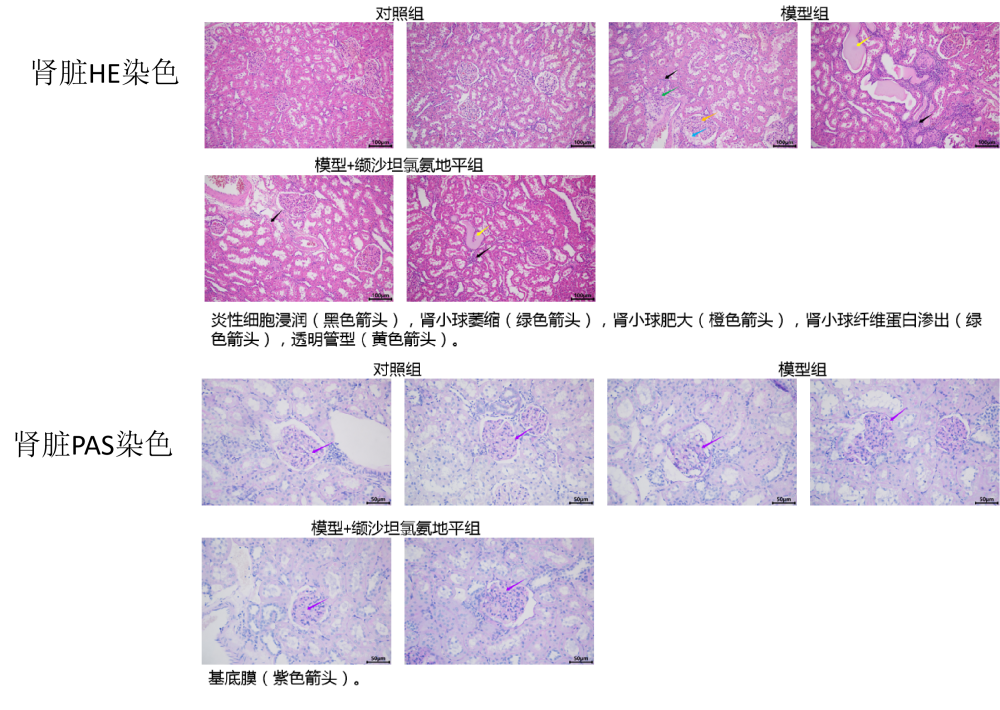
参考文献:
1. 高血压
2. Stephanie Randar,Diana L. Silva-Velasco,Fernanda Priviero,R. Clinton Webb,RhoA/Rho-Kinase Signaling in Vascular Smooth Muscle and Endothelium: Mechanistic Insights and Translational Implications in Hypertension, Biomolecules, 15, 11, (1607), (2025).https://doi.org/10.3390/biom15111607
3. 临床进展检索结果 - 全球新药竞争情报库
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
