2025肥胖药研发“狂飙”——顶刊引领,药企竞逐
2025年,《柳叶刀》等国际顶尖学术期刊发布一系列颠覆性肥胖机制研究,欧洲糖尿病研究协会年会(EASD)展示靶点药物最新成果,礼来、恒瑞医药等国内外药企纷纷加快临床转化进程。顶刊的前沿洞察与产业端的落地动态,共同勾勒出下一代肥胖药物的核心竞争版图。

图源:中洪博元
1. 脂-脑通讯:改写肥胖认知的新发现
11月11日,南京大学毕艳教授团队在Cell 子刊《细胞・代谢》发表Adipocyte-derived extracellular vesicles are key regulators of central leptin sensitivity and energy homeostasis,首次揭示脂肪组织分泌的细胞外囊泡(EVs)及其携带的微小核糖核酸(miRNAs)是调控大脑瘦素敏感性的关键“信使”。正常情况下,它们能穿越血脑屏障增强瘦素信号,抑制食欲、加速能量消耗;肥胖时这类miRNAs减少,导致大脑瘦素敏感性下降,进而引发体重增加。基于此研究团队创新性地打造了脑靶向外泌体递送系统,可精准递送促瘦素增敏miRNAs,重新激活瘦素信号。
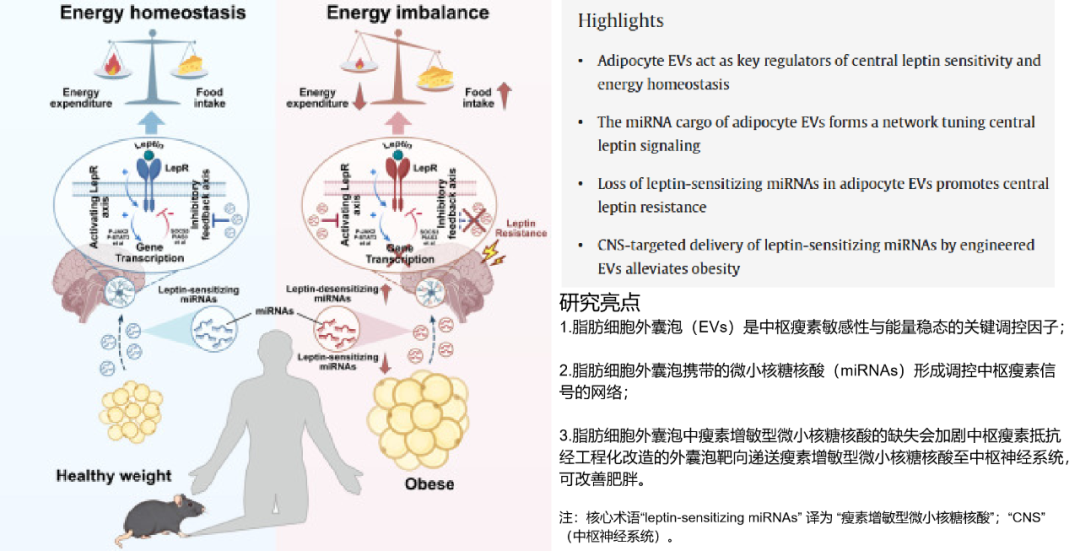
图源:Cell Metabolism
这一成果不仅在理论上为肥胖发病机制的研究提供了全新的视角,将瘦素抵抗的研究从传统的“以大脑为中心”模式转向“器官间通讯”框架,也为药企在肥胖药物研发领域解锁了“器官间通讯调控”这一极具潜力的创新赛道。
2. 多靶点叠加,解锁新效能
2025欧洲糖尿病研究协会年会(EASD)上刚公布的GLP-1 R/GIPR/ 泛PPAR五重激动剂,它特别巧妙地整合了多种优势机制——结合 GLP-1R/GIPR 共激动的“减重+降糖” 功效与PPAR激动的 “提胰岛素敏感性+调血脂”作用,实现代谢改善的协同增效。药物设计方面,选择lanifibranor作为泛PPAR激动剂,激活三种 PPAR 亚型(α、δ 和 γ)。更为独特的是,这个五重激动剂中的泛PPAR部分能够精准地递送到表达GIP或GLP-1受体的细胞上,避免药物在其他细胞中不必要的作用,从而大大提高药物疗效,降低潜在副作用。
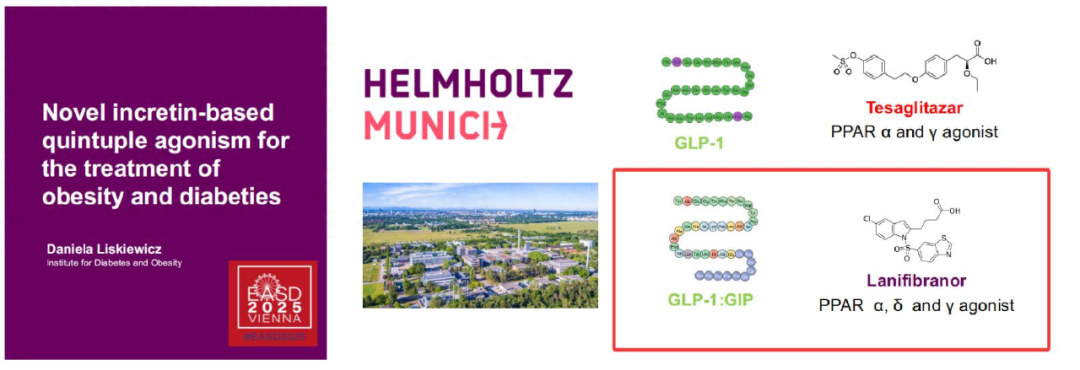
图源:EASD
动物实验里这个五重激动剂不管是减体重、控食欲,还是改善肥胖小鼠的高血糖和胰岛素抵抗等代谢指标上,效果都很突出。它的存在破解GLP-1类药物效能快到极限的行业难题!这种 “机制叠加+靶向递送”的创新思路,给代谢病药物研发指了新方向,其转化潜力和合作空间让人期待。
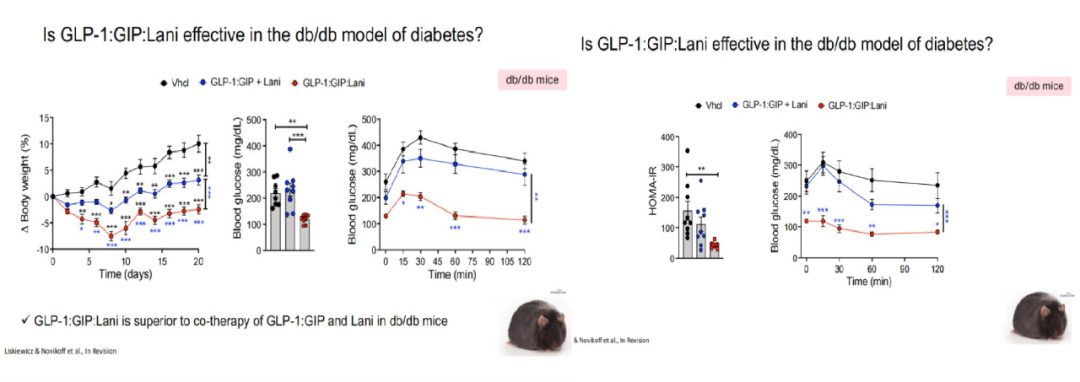
图源:EASD
3.产业动态:临床转化的加速推进
2025年11月6日,美国Endeavor Health与礼来公司在《柳叶刀》期刊发表一项2期临床研究,直观呈现了“高选择性+剂量调控”的单靶点药物优化研发逻辑。

图源:The Lancet
这款新型药物Eloralintide(选择性胰淀素受体激动剂),高选择性作用机制是其疗效落地的关键基石。在为期48周的对照试验中,纳入263名18-75岁无糖尿病的肥胖/超重成年人,所有Eloralintide治疗组的表现均显著优于安慰剂组。其中,9mg固定剂量组与6 - 9mg剂量递增组脱颖而出,均成功实现20%的平均体重下降。为了深入探索用药的安全性与有效性,研究中特意设置固定剂量(1mg、3mg、6mg、9mg)与两种剂量递增(6 - 9mg、3 - 9mg)方案。巧妙验证从9%到20%的减重效果梯度,更通过剂量递增模式成功优化用药安全性。
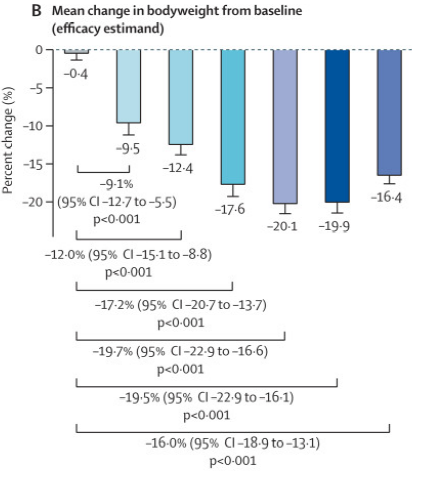
图源:The Lancet
此“以高选择性锁定作用靶点,用灵活剂量调控平衡疗效与安全性”的研发思路,不仅实现了强效减重,更带来腰围缩小、血脂及血糖指标改善等额外获益。值得关注的是,礼来将于12月正式启动Eloralintide的3期临床试验,有望成为全球首个上市的高选择性AMY1R激动剂,这也意味着该研发思路正进入更深入的验证阶段。这无疑提供了极具参考价值的实用方向:在聚焦靶点选择性的基础上,通过精细化剂量设计,可显著提升药物的临床竞争力。
2025年11月美国肥胖周大会上,恒瑞医药自主研发的国内首个GLP-1/GIP双受体激动剂HRS9531,其Ⅲ期临床研究数据重磅亮相。该研究6mg剂量组治疗48周后与Ⅱ期临床8mg 组23.6%的平均减重成果一致,均呈现减重未达平台期的优异态势,预示着更长周期治疗下的潜力空间。目前,该药物已递交新药上市申请并获国家药监局受理,而其合作方美国Kailera公司(前身是“Hercules CM NewCo”)计划于年底前启动全球Ⅲ期临床,全力推进HRS9531的全球化布局。
信达生物自主研发的玛仕度肽,于今年10月底公布Ⅲ期临床试验(全球首个与司美格鲁肽头对头比较)DREAMS-3阳性结果,证明核心临床终点优于司美格鲁肽,实力堪称强劲!值得关注的是,玛仕度肽的研发节奏全程展现出跨越式提速:2023年12月启动DREAMS-3试验,实现Ⅱ期向Ⅲ期的无缝衔接;2024年短短9个月内,3项核心Ⅲ期试验接连达标,同步推进上市申报;2025年6月获批后迅速落地临床。整个 DREAMS-3试验仅用22个月便完成全部流程并公布结果,较全球同类试验显著提速,一举创下国产GLP-1类药物研发的最快纪录。

图源:环球网
石药集团、华东医药等也紧锣密鼓布局,形成多点开花竞争格局。石药集团司美格鲁肽注射液于2025年8月5日获国家药监局上市申请受理,其体重管理适应证已完成Ⅲ期临床入组,长效制剂SYH9017也已获批临床;GLP-1类创新药依达格鲁肽α注射液(TG103)已提交新药上市申请。华东医药司的美格鲁肽于2025年3月31日获上市申请受理,体重管理适应证2025年2月完成Ⅲ期临床入组;口服小分子GLP-1受体激动剂HDM1002已完成体重管理适应证Ⅲ期入组,双靶点激动剂HDM1005的糖尿病及体重管理适应证Ⅱ期临床均已完成入组,三靶点激动剂DR10624多项Ⅱ期临床已启动。
能明显感觉到,在肥胖药物赛道上,这些本土企业,一边持续砸钱搞研发,一边主动对接国际前沿,跟国际药企的差距正在一点点缩小。现在这行的发展节奏太快了,学术研究不断解锁新的治疗方向,实验室成果向临床实用产品的转化速度正以肉眼可见的态势加速推进。
中洪博元肥胖症模型介绍——小鼠肥胖症模型
肥胖症是一种由多种因素引起的慢性代谢性疾病,表现为体内脂肪堆积过多和(或)脂肪分布异常,通常伴有体重增加。
造模:5周龄BALB/c 雄性小鼠适应性饲养1周,正常组给予普通饲料喂养 14 周,自由饮水。模型组给予高脂饲料喂养 14 周,自由饮水。
造模周期:14周
阳性药物:司美格鲁肽注射液;奥利司他胶囊
模型验证
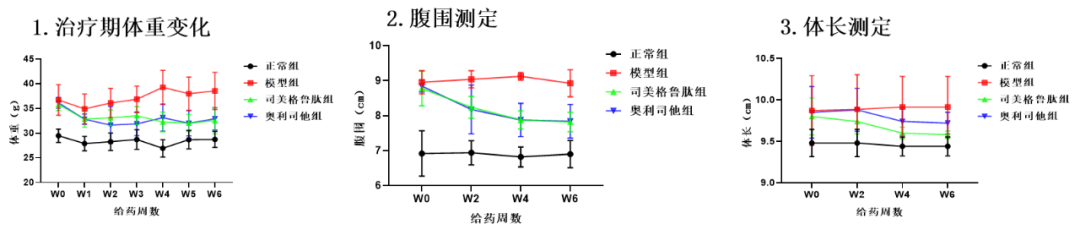
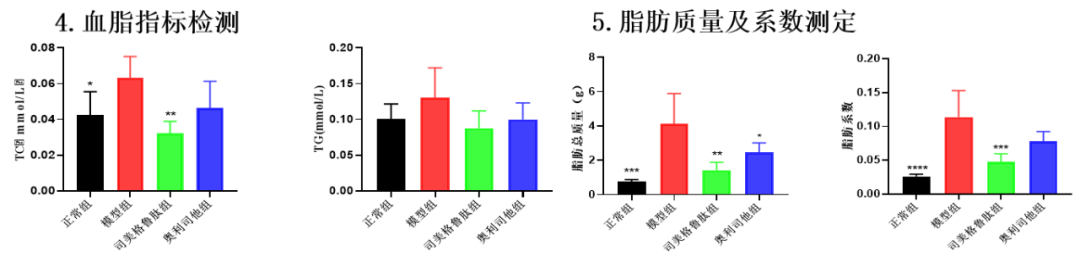
参考文献:
【1】Wang J, Zhang X, Zhu Y, Sun H, Chen X, Zhao Z, Zhang N, Zhang C, Li L, Bi Y. Adipocyte-derived extracellular vesicles are key regulators of central leptin sensitivity and energy homeostasis. Cell Metab. 2025 Nov 11:S1550-4131(25)00439-5. doi: 10.1016/j.cmet.2025.10.005. Epub ahead of print. PMID: 41223857.
【2】Billings LK, Hsia S, Bays H, Tidemann-Miller B, O'Hagan J, Tham LS, Butler A, Kazda C, Mather KJ, Coskun T. Eloralintide, a selective amylin receptor agonist for the treatment of obesity: a 48-week phase 2, multicentre, double-blind, randomised, placebo-controlled trial. Lancet. 2025 Nov 6:S0140-6736(25)02155-5. doi: 10.1016/S0140-6736(25)02155-5. Epub ahead of print. PMID: 41207310.
免责声明:本文内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司专业从事药物研发临床前CRO服务,公司构建了从疾病模型制备→药效药理→病理检测→生化检测→结果报告一体化服务。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
中洪博元成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
如想了解实验详情欢迎咨询:
💬 关注微信公众号「中洪药效评价」咨询
