突破治疗瓶颈!戈谢病创新疗法研发迎来新征程
戈谢病(Gaucher Disease,GD)是一种罕见的常染色体隐性遗传溶酶体贮积症,由GBA基因缺陷导致葡萄糖脑苷脂酶活性缺乏,使葡萄糖脑苷脂在巨噬细胞内异常贮积,累及肝、脾、骨髓、中枢神经系统等多个器官,严重威胁患者生命健康。根据神经系统受累情况,戈谢病主要分为三型:GD1型(非神经型)最为常见,仅累及内脏和骨髓;GD2型(急性神经型)发病凶险,婴儿期起病且快速进展,多在2岁内夭折;GD3型(神经内脏型)儿童或青少年期起病,兼具内脏损害与渐进性神经病变,预后中等且随神经症状加重而变差。据统计,戈谢病的全球发病率仅为1/10万,我国人群患病率仅为1/50万~1/20万,已列入我国《第一批罕见病目录》。
图源于网络
长期以来戈谢病的临床主流治疗为酶替代治疗(ERT)和底物减少治疗(SRT),但存在诸多局限:ERT需长期静脉输注、依从性低,且无法改善GD3型神经病变;SRT疗效有限、难控长期病情,还存在患者不耐受情况。近年来医药研发技术迭代,戈谢病创新药研发迎来爆发,口服靶向药、基因治疗等药物相继问世,覆盖不同亚型,让治疗从“对症缓解”稳步迈向“精准根治”,为患者带来新希望。
壹
核心突破:直击GD3型神经病变
GD3型进行性神经系统病变是戈谢病治疗的最大临床瓶颈,传统 ERT 药物因无法穿透血脑屏障,难以缓解患者的共济失调、认知减退等神经症状,最终可致患者丧失生活能力。2026年2月,赛诺菲公布Venglustat的LEAP2MONO三期临床试验成果,这款创新药成为首个在神经症状改善上优于传统 ERT 疗法的药物,有望填补GD3 型神经病变治疗的全球空白。
Venglustat是一款新型口服葡糖基神经酰胺合成酶抑制剂(GCSi),其核心优势在于具备良好的血脑屏障穿透性,能够直接进入中枢神经系统,从根源上抑制葡萄糖脑苷脂的异常合成与贮积,同时兼顾全身症状控制,且每日一次的口服给药方式,大幅提升了患者的用药依从性,摆脱了传统ERT药物长期静脉输注的困扰。

图源于赛诺菲
该三期临床为双盲、双模拟、主动对照设计,纳入43名12岁及以上、经至少3年 ERT治疗且全身症状达标的GD3型患者,1:1分至 Venglustat口服组与ERT静脉输注对照组。治疗52周后,Venglustat组达成所有预设主要终点,神经功能评估疗效显著优于ERT疗法,对全身脏器及血液学指标的控制效果则与标准治疗相当。
基于此阳性结果,赛诺菲计划在全球提交Venglustat用于3型戈谢病的上市注册申请。该药已在欧、美、日获孤儿药资格认定,还得到美国FDA快速通道资格认定,其三期临床的成功不仅为GD3型戈谢病患者带来新希望,也为其他伴神经病变的溶酶体贮积症药物研发提供了重要借鉴。
贰
AAV基因突破GD1型治疗局限
除了口服靶向药的突破,基因治疗作为“根治性”疗法的探索,也取得重大进展。近日,在美国圣地亚哥举办的第22届WORLDSymposiu年会上,Spur Therapeutics公司公布了其用于治疗Ⅰ型戈谢病的在研AAV基因疗法FLT201的 I/II期临床研究最新数据。
FLT201采用自主研发的肝脏靶向AAVS3载体,搭载经工程化改造、稳定性更高的β- 葡萄糖脑苷脂酶变体功能基因,能让患者干细胞内持续补充缺失的葡萄糖脑苷脂酶,高效降解异常贮积的糖脂及毒性代谢物,从根源解决酶缺乏问题,有望实现“一次治疗,长期获益”的治疗目标。

FLT201载体设计
本次公布的数据来自GALILEO-1 I/II期试验和GALILEO-2长期随访研究,入组患者均接受过至少2年的ERT/SRT标准治疗。其中4名接受FLT201单次低剂量治疗的患者,均在11周内停用原有疗法,截至2025年11月数据截止日,已持续停药20-26个月。治疗后患者的核心生物标志物和临床指标均获持久改善:溶酶体葡萄糖鞘氨醇在两年随访中显著下降53%-94%;骨髓底物蓄积这一难治问题实现突破,有患者该指标被完全清除;血红蛋白、血小板计数及肝脾体积也均保持改善或稳定,患者彻底摆脱传统疗法的频繁治疗负担。
基于优异的 I/II 期数据,Spur公司已启动FLT201的全球多中心III期临床研究,且与美国FDA就单臂试验设计达成共识,该成果有望同时支持药物的加速审批与完全审批,为其早日上市奠定坚实基础。
叁
国产ERT新药获批上市,填补国内空白
在口服靶向药和基因治疗稳步推进的同时,国产酶替代治疗(ERT)新药也实现重大突破,北海康成研发的注射用维拉苷酶β(商品名:戈芮宁®)于2025年5月15日获NMPA批准上市,成为中国首个戈谢病ERT新药,适用于12岁及以上青少年和成人1型、3型戈谢病患者的长期治疗,填补了国内领域空白,打破进口ERT药物垄断,大幅提升治疗普惠性。
戈芮宁®的上市极具里程碑意义,其研发审批全程高效推进:2024年8月公布关键临床试验积极顶线数据,9月获CDE优先审评资格,11月新药上市申请被正式受理;2025年3月通过注册核查与上市前GMP符合性检查,5月正式获批,彰显了我国罕见病新药研发与审批的提速成效。
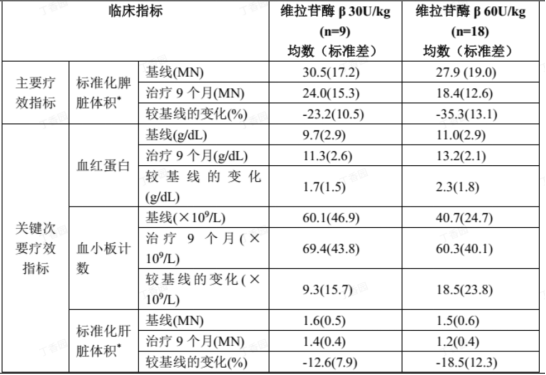
图源于丁香园
该药物的关键性临床试验为随机、双盲、剂量比较研究,评估了每2周一次静脉滴注在初治患者中的疗效、安全性与药代动力学,且设有开放标签扩展期。结果显示,60U/kg和30U/kg两个剂量组均成功达到主要疗效终点,治疗9个月后受试者脾脏体积较基线平均缩小,疗效不逊于进口ERT药物,且安全性良好。作为一类创新药,戈芮宁®研创全链条积累了完整数据,上市后将大幅降低治疗成本,打破进口药价格壁垒,让更多普通家庭患者负担得起规范治疗,真正实现戈谢病治疗的普惠化。
肆
展望
未来,戈谢病治疗将持续向精准化、长效化和普惠化发展,靶向与基因治疗的研发突破将进一步突破传统治疗瓶颈,推动从对症缓解向根源性治疗跨越。同时国产创新药的落地与迭代,将不断提升药物可及性、降低治疗成本,逐步建立覆盖不同亚型的优质治疗体系,也为其他罕见病诊疗研发提供宝贵经验,让更多罕见病患者迎来更好的治疗前景。
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
