突破耐药困局!肝癌靶向与免疫治疗迎来多维革新
作为全球第二大癌症死亡原因,肝癌(尤其肝细胞癌 HCC)防控形势严峻。我国是肝癌负担最重的国家,可手术患者术后5年复发转移率高达60%~70%,晚期患者5年生存率不足20%。近年,《Nature》《柳叶刀》等顶刊连续发表突破性成果,ACLY、FGFR4等新靶点被揭示,联合治疗方案迭代升级,叠加药企管线快速推进,为肝癌精准诊疗开辟全新路径。
核心靶点突破
ACLY代谢靶点:重塑MASH-HCC免疫微环境
代谢功能障碍相关脂肪性肝炎(MASH)已成为肝癌新诱因,其驱动的肝癌具有独特免疫抑制微环境,对传统免疫治疗耐药。2025年《Nature》研究首次证实,ATP-柠檬酸裂解酶(ACLY)是连接肿瘤代谢与免疫调控的关键靶点。

图源:nature
核心机制:ACLY通过增强脂质生物合成支撑癌细胞增殖,同时生成乳酸等免疫抑制产物。基因抑制ACLY可使MASH-HCC小鼠肿瘤病变减少70%以上;新型小分子抑制剂EVT0185通过结合ACLY辅酶A位点发挥作用,单药治疗显著降低肿瘤负荷,还能增强酪氨酸激酶抑制剂与免疫疗法的疗效。其抗肿瘤效应依赖B细胞浸润及三级淋巴结构形成,B细胞耗竭可完全阻断药物作用,为免疫联合代谢干预提供理论依据。目前EVT0185已进入临床前后期开发,成为药企布局MASH-HCC领域的核心管线方向。
FGFR4靶点:晚期耐药肝癌的精准突破
晚期肝癌患者经靶免治疗进展后缺乏有效后续方案,成临床亟待解决的痛点。2025年,华中科技大学同济医学院附属同济医院牵头启动全球首个FGFR4靶向药物ABSK-011的关键性临床研究,为耐药患者带来新希望。

图源:tjh
核心机制:FGFR4通路异常活化是肝癌发生发展的“分子开关”,全球尚未有该靶点药物获批。ABSK-011具有高选择性抑制FGFR4的独特分子结构,I期研究显示,在经靶免治疗进展的FGF19阳性患者中,客观缓解率(ORR)达44.8%,中位无进展生存期(PFS)达5个月,安全性良好,首次实现肝癌从驱动基因检测到靶向干预的完整闭环。目前由上海和誉医药推进关键性临床,聚焦FGF19阳性人群,开创精准治疗新策略。
circSMEK1靶点:阻断MASH向肝癌进展
MASH向肝癌进展机制特殊,部分可跳过肝硬化阶段,传统干预手段效果有限。2025年《Advanced Science》研究揭示,环状RNA circSMEK1是抑制该进程的关键靶点,兼具诊断与治疗价值。

图源:advanced
核心机制:circSMEK1通过hnRNPK-IGF2-AKT轴发挥肿瘤抑制作用,其血清水平对HCC无创诊断的曲线下面积(AUC)达0.790,对早期HCC及高危MASH亦有潜在诊断价值。动物实验中,恢复circSMEK1可显著抑制肿瘤生长转移,联合IGF2抑制剂疗效更佳,相关干预策略已进入药企早期研发管线,聚焦MASH相关肝癌的一级预防。
临床转化升级
替雷利珠单抗联合仑伐替尼:围术期高复发风险肝癌新方案
免疫联合靶向治疗在晚期肝癌疗效显著,但围术期应用价值亟待验证。近日,天津医科大学肿瘤医院陈璐副主任医师为第一作者,宋天强教授团队在《Nature Communications》发表研究成果,为高复发风险可切除肝癌提供新路径。

图源:nature
该前瞻性单臂Ⅱ期临床试验,系统评估了PD-1抑制剂替雷利珠单抗联合仑伐替尼在围术期的安全性与疗效,同时构建人工智能疗效预测模型。研究证实该方案可行性优异,可有效降低术后复发风险,为临床筛选获益人群、优化围术期治疗策略提供循证依据。郝继辉教授、宋天强教授、李咏梅教授为共同通讯作者。
“双艾”方案:围术期治疗实现疗效翻倍
2025年《柳叶刀》发表的CARES-009 Ⅲ期研究,为可切除肝癌围术期治疗带来里程碑突破,中国原研方案登顶国际顶刊。该研究由樊嘉院士指导、周俭教授牵头,采用恒瑞医药“双艾”方案(卡瑞利珠单抗+阿帕替尼)构建“新辅助+手术+辅助”三明治疗法。

图源:thelancet
结果显示,相较于单纯手术,该方案使患者中位无事件生存期从19.4个月延长至42.1个月,显著降低复发转移风险,标志着肝癌治疗进入“追求治愈”的慢病化管理时代,有望推动全球诊疗指南更新,彰显中国原研药的全球竞争力。
GPC-3靶向RDC:肝癌精准诊断新突破
早期诊断不足与复发监测困难是肝癌生存率偏低的重要原因。2025年,远大医药公布GPC-3靶向诊断型放射性核素偶联药物(RDC)GPN02006的IIT临床突破,为精准诊断提供新工具。
图源:grandpharm
该药物对GPC-3靶点具有高特异性亲和力,给药后30分钟即可实现高质量显像,背景信号极低、病灶摄取特异性强,在微小病灶检测、治疗反应评估及复发预警中优势显著,且安全性优异无药物相关不良反应。目前有望成为全球首个GPC-3靶点HCC诊断类RDC,远大医药同步布局同靶点治疗类RDC,推进肝癌诊疗一体化。
总结
当前肝癌研究已形成“代谢调控-微环境重塑-临床转化”的完整链条,尽管仍面临靶点异质性、耐药性等挑战,但随着多组学技术、空间成像与AI药物研发的深度融合,“靶向+免疫+局部治疗”多模态方案将持续优化。
未来,随着更多创新药上市与医保准入,肝癌患者生存获益将持续提升,攻克“癌中之王”的愿景正逐步落地。
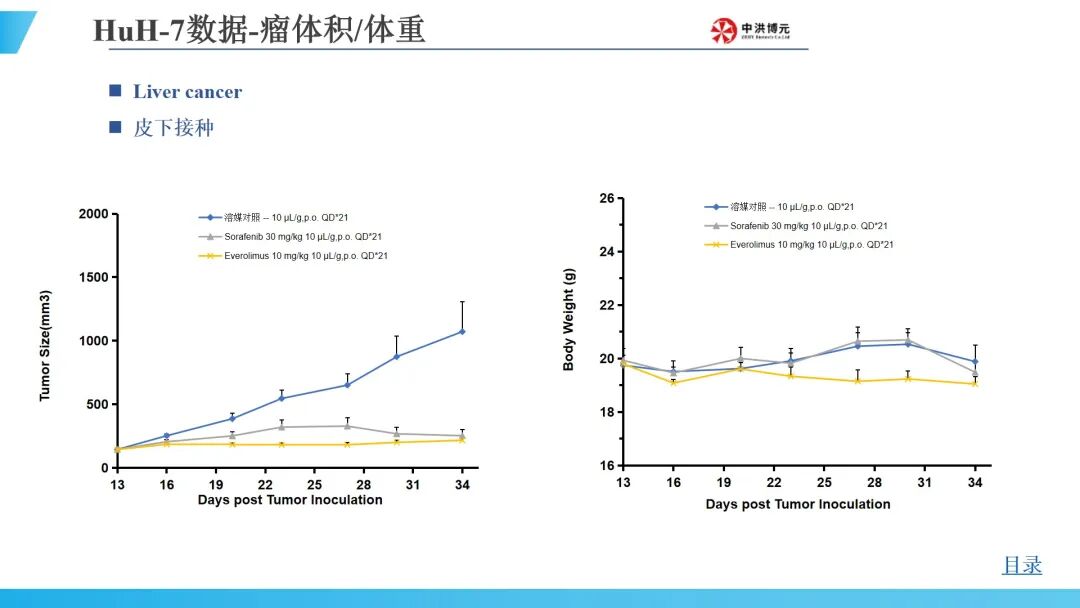
中洪博元肝癌模型
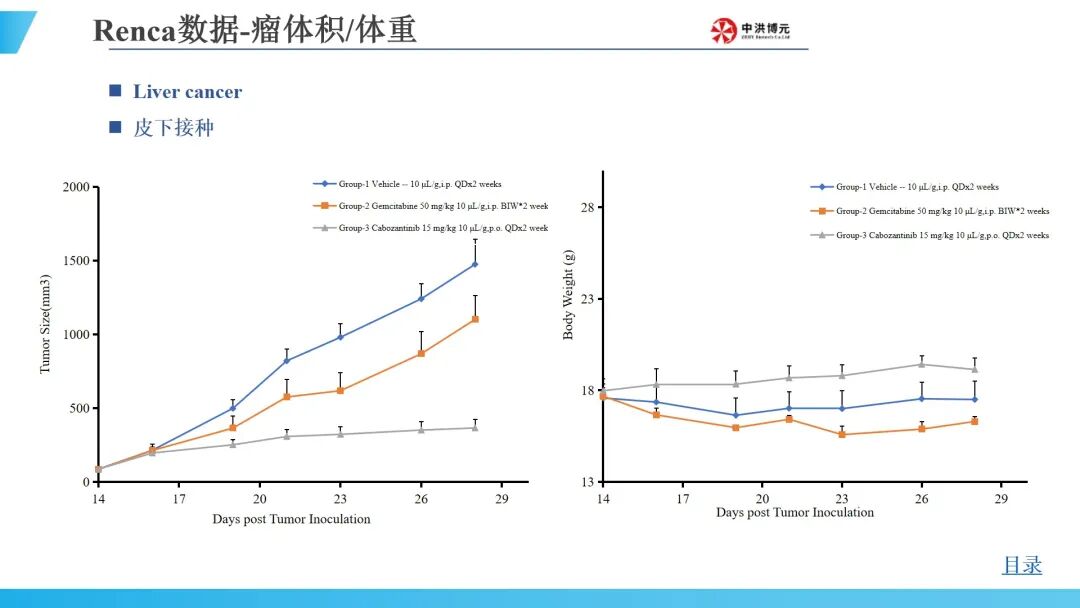
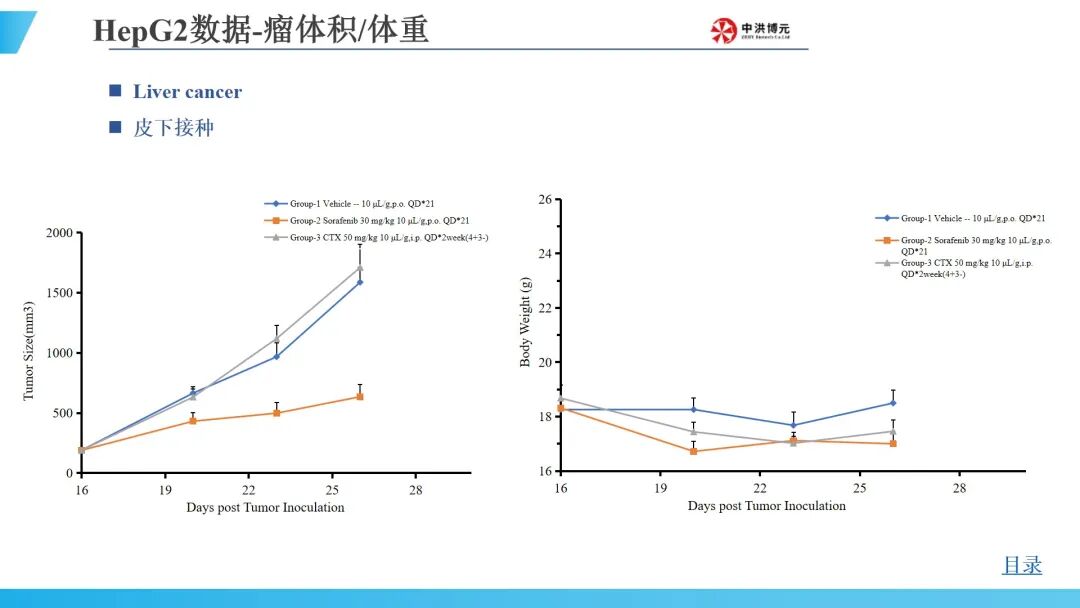
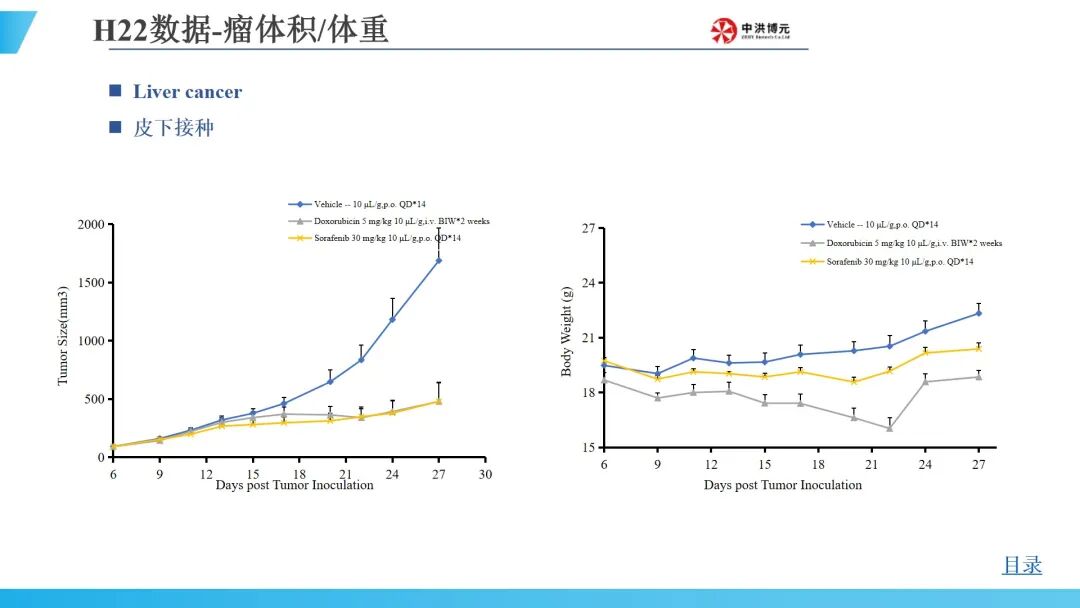
免责声明:本文内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
