动脉粥样硬化研究2025年终盘点:从全新机制到新药上市,防线再升级
动脉粥样硬化(AS),作为心梗、脑梗等致命心血管事件的“元凶”,长期以来都是全球医学研究的重中之重。2025年末,国内团队接连在顶级期刊揭示发病新机制,而全球多款靶向降脂、抗炎、斑块逆转的新药也加速落地中。
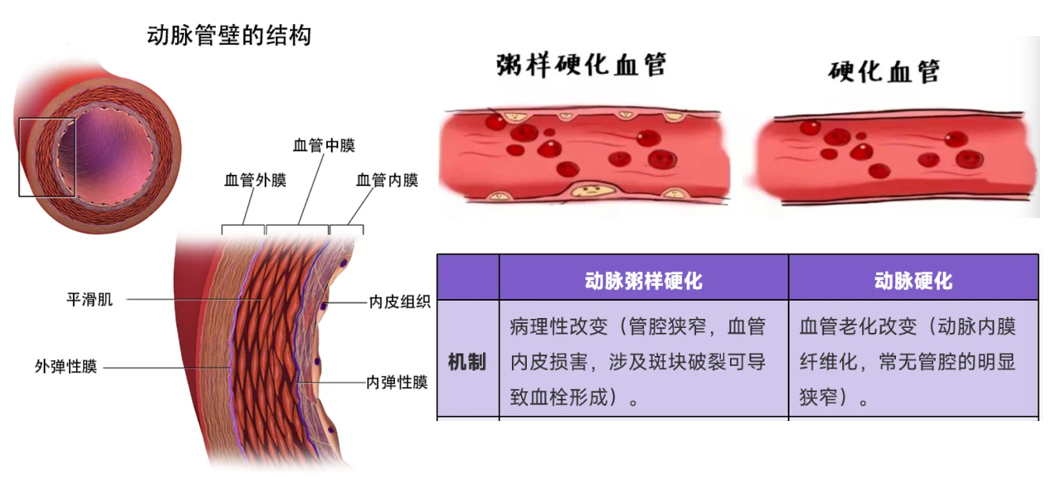
图源:贾钰华教授&丁香园
基础研究突破:解锁动脉粥样硬化新密码
近期,重庆医科大学孙阳教授、黄荣忠教授团队联合昆明理工大学蒋立虹教授团队,在动脉粥样硬化发病机制研究领域接连取得重大突破,为相关新药研发提供了全新的靶点方向。
2025年12月3日,团队在Cell Reports发表的研究“Interleukin-1/Toll-like receptor signaling potentiates macrophage olfactory receptor 2-driven atherosclerosis”,首次阐明嗅觉受体OR6A2在动脉粥样硬化进展中的关键作用。嗅觉受体传统认为主要存在于鼻腔,而该研究首次发现其在血管巨噬细胞中存在功能性表达,且激活后会显著加剧炎症反应,直接推动动脉粥样硬化发展。研究进一步明确,OR6A2的配体——辛醛(一种脂质过氧化产物)可在氧化低密度脂蛋白中检测到,而氧化低密度脂蛋白本身就是动脉粥样硬化的核心危险因素之一。值得关注的是,支架蛋白β-抑制蛋白2(βarr2)是炎症调控的“天然刹车手”:它通过与OR6A2结合促进其内吞内化(即“关闭”OR6A2活性),进而抑制巨噬细胞内NLRP3炎症小体激活(炎症是动脉粥样硬化斑块形成的核心驱动力),最终减少促炎因子释放,延缓病变进展。
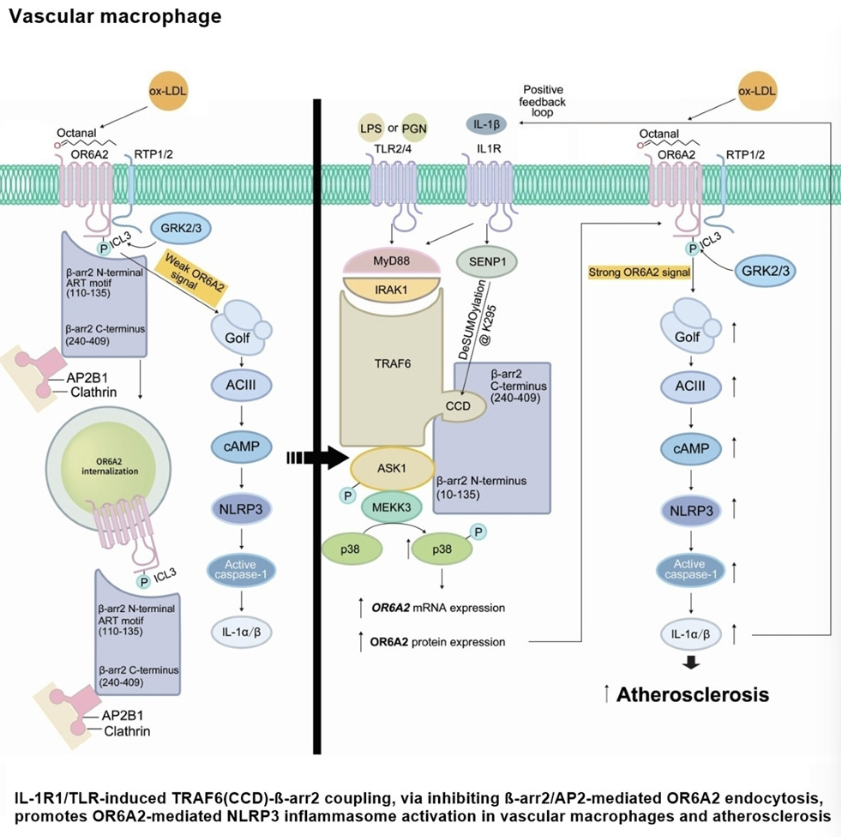
图源:Cell Reports
IL-1R1/TLR信号通路可促使肿瘤坏死因子受体相关因子6(TRAF6)的卷曲螺旋结构域与βarr2结合,阻断βarr2与OR6A2的相互作用,导致OR6A2持续“活跃”,最终加剧炎症反应和动脉粥样硬化病变,而研究中在血管巨噬细胞中阻断TRAF6与βarr2的结合,有效抑制小鼠模型的动脉粥样硬化发展,这为精准治疗提供了明确的靶点方向。
此前,该团队已于2025年3月4日在PNAS发表研究“The RNA-binding protein RBPMS inhibits smooth muscle cell–driven vascular remodeling in atherosclerosis and vascular injury”,发现另一个关键调控因子——RNA结合蛋白RBPMS。RBPMS是血管平滑肌细胞(VSMC)特异性的保守基因,而动脉粥样硬化及血管壁损伤引发的VSMC表型异常,是血管重构、斑块帽生长及介入治疗后再狭窄的重要诱因。研究证实,RBPMS可通过与心肌素(MYOCD)前体mRNA相互作用,借助替代性外显子2a剪接增强MYOCD_v3/MYOCD_v1转录本平衡,以MYOCD_v3a依赖的方式促进VSMC收缩表型分化、降低其纤维增生活性。这一机制能有效抑制VSMC驱动的血管重构,减少斑块帽发展及介入后内膜增生。
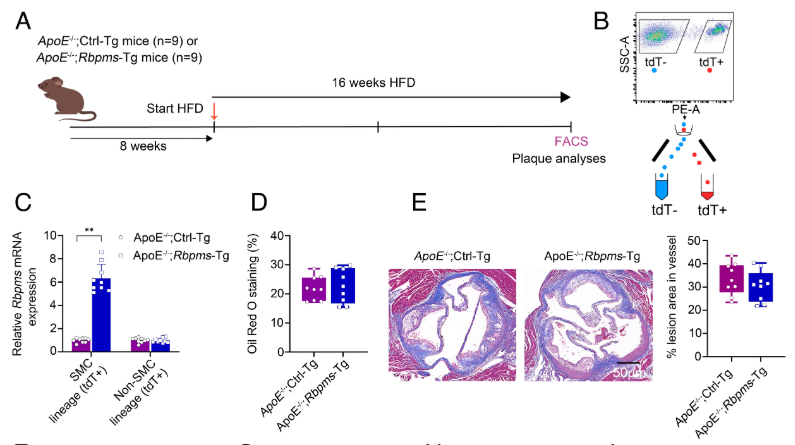
图源:PNAS
基于以上研究成果,该疾病部分药物研发未来可重点锚定两核心方向:1)巨噬细胞炎症通路的靶向干预,围绕OR6A2、TRAF6、βarr2等核心靶点;2)血管平滑肌细胞(VSMC)的表型调控,聚焦RBPMS、MYOCD这类关键靶点。此外,可依托成熟的体外细胞模型、小鼠模型等体系开展系统的临床前研究。也可以尝试走联合应用的路径,或借力“抗炎+抗血管重构”的双重叠加效应,放大治疗价值,向突破性疗法的申报方向发力。另外针对RBPMS这条特色通路,还可以尝试打造「介入治疗+靶向药物」组合,精准瞄准血管修复、血管再狭窄防治这一细分赛道,凭借这种差异化的研发思路和产品布局,形成核心竞争力。
临床研发:多款新药落地
目前,动脉粥样硬化相关新药研发聚焦降脂、抗炎、斑块逆转、中医药协同等核心方向,多款新药获批或进入关键临床阶段。
12月17日,云顶新耀-B(01952.HK)股价显著拉升,截至收盘,涨幅为6.79%,报50港元/股。该股大幅异动,主要源于云顶新耀·乐瑞泊®(通用名:lerodalcibep-liga)于2025年12月12日获FDA批准,用于成人高胆固醇血症(包括杂合子型家族性高胆固醇血症HeFH)。作为首个PCSK9抑制剂融合蛋白,其Ⅲ期数据显示,心血管高风险人群LDL-C(坏胆固醇)持续下降≥60%,HeFH患者下降59%;中国关键注册Ⅲ期已完成12周数据分析,达到主要疗效终点。目前云顶新耀通过与海森生物的授权协议获得大中华区独家许可,拟2026年上半年递交BLA,最快2027年在国内获批,同时已向欧洲药品管理局(EMA)递交上市申请。随着此次FDA批准落地,叠加大中华区商业化进程的推进,云顶新耀有望借助乐瑞泊这款重磅产品,拓展至具有庞大未满足需求的心血管治疗领域,为长期业绩增长注入强劲动力。

图源:新药情报库
默沙东·Enlicitide的口服PCSK9抑制剂,打破传统PCSK9抑制剂需注射的局限。2025年11月公布的两项Ⅲ期研究均获阳性结果,24周降LDL-C约60%,一年疗效稳定,患者依从性高达97%,有望成为降脂治疗的新选择。
新元素药业ABP-745的靶向NLRP3炎症小体(口服抑制剂),12月16日获FDA批准启动Ⅱ期全球多中心试验。临床前数据显示,其安全窗优于传统抗炎药秋水仙碱,单药可降低主动脉斑块面积56.1%,联用他汀类药物降幅超75%,能覆盖炎症全周期,潜力巨大。值得一提的是,新元素药业已递交上市申请,聚焦代谢、炎症及心血管疾病领域。
全球首款进入临床试验的动脉粥样硬化靶向斑块逆转药物,12月获FDA同意以“斑块逆转”作为加速批准替代终点,开展Ⅱb期关键注册性临床。这是美国FDA历史上第一次采用替代终点(RLSE)获批心血管新药,这份殊荣给到了一家中国公司——茵诺医药YN001。其Ib/IIa期临床数据已于2025年欧洲心脏病学会年会(ESC 2025)全球首发,结果显示接受治疗的患者冠状动脉总斑块体积(TAV)降幅达10%-50%,斑块体积百分比(PAV)降幅达10%-30%,颈动脉及外周血管斑块面积也明显缩小。该药物有望大幅降低患者心血管事件风险。茵诺医药拟1年多完成关键临床并申报加速批准,若试验成功,有望快速上市为斑块逆转提供针对性药物。
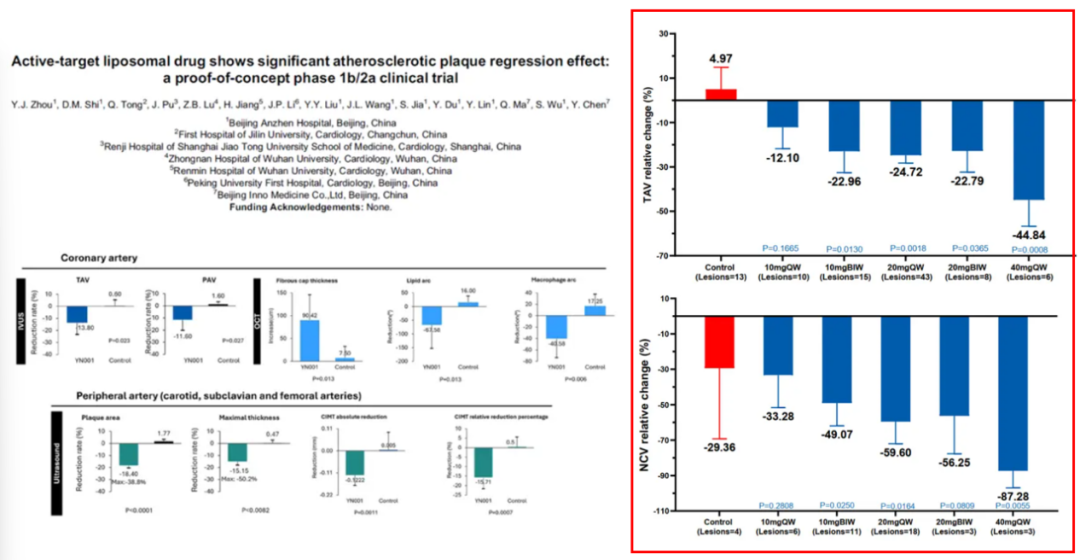
图源:网易新闻&医药魔方
正大青春宝·冠心宁片:12月12日通过药物临床试验登记与信息公示平台公示启动Ⅱ期临床(CTR20254709),试验状态为进行中(尚未招募),目标入组100人。该研究用药52周,主要评估其对动脉粥样硬化性心血管疾病(ASCVD)伴颈动脉易损斑块的有效性,核心终点为富脂质坏死核心(LRNC)体积、LRNC最大面积百分比较基线的变化,同时将评估降低心血管风险等次要终点。
红云制药·绞股蓝总苷胶囊:12月启动国家级重大专项临床,通过联合阿托伐他汀干预颈动脉斑块,旨在提供中医药防治ASCVD的高级别循证证据。该药物传统适用于高血脂症,针对心脾气虚、痰阻血瘀引发的心悸气短、胸闷肢麻等症状,此次研究将为不耐受他汀或血脂达标难的患者提供新的联合方案。
梳理今年年末的各项研究进展,动脉粥样硬化治疗呈现四大明确趋势:1.多靶点协同:从单一降脂转向“降脂+抗炎+斑块稳定/逆转”;2.给药方式多口服,少注射制剂;3.中西医融合:通过高级别循证研究验证中医药的治疗价值,形成中西医协同方案;4.替代终点突破:例如YN001获FDA认可“斑块逆转”作为加速批准终点,大幅缩短研发周期,能更快惠及患者。
从国内团队揭示的嗅觉受体、RNA结合蛋白等全新发病机制,到多款新药加速落地,2025年的动脉粥样硬化研究随着基础研究与临床转化的深度融合,未来有望形成“靶点精准+中西医协同”的防治体系,为亿万心血管疾病高风险人群筑起更坚固的健康防线。期待这些研究成果更快落地,惠及更多患者!
中洪博元动脉粥样硬化模型介绍
造模:高脂饲料喂养兔/鼠建立动脉粥样硬化模型,阳性药物为阿托伐他汀。
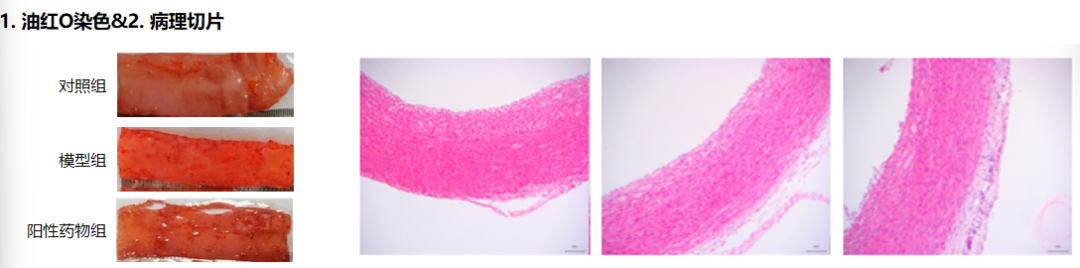
模型对照组与空白组明显不同。而红色的深浅来看,阿托伐他汀组均对粥样硬化有治疗效果。模型组的内皮下层增厚,有一些较均匀分布的小斑块(着色浅),内膜细胞排列比较紊乱。阳性药物组能减少空泡细胞的出现。
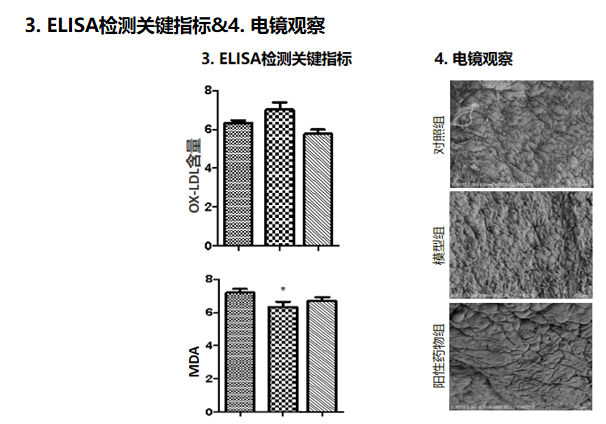
正常血管内皮不吸附白细胞,但是高胆固醇饮食的动物模型,早期血管内皮表面就能吸附多种白细胞的黏附分子。
免责声明:本号内容仅供读者学习和交流。文章、图片等版权归原作者享有,如有侵权,请留言联系。
关于中洪博元
江西中洪博元生物技术有限公司成立于2015年,11年来坚持大规模标准化创制人类疾病动物模型,开展更接近人类疾病发生发展机制、更有临床转化价值的原创动物模型技术攻关,目前,中洪博元已合作药企200余家,开展项目300余项,积累了丰富的药理药效项目经验。
中洪博元秉承助力新药研发理念,开展基于动物疾病模型的药效研究,拥有获得AAALAC完全认可的实验平台。公司配备了全种类实验场地,大小鼠SPF级标准实验室3000平米,猪、犬、羊、兔大动物实验室4000平米,检测中心5000平米。平台使用SPF级动物,配备10万级洁净度屏障环境,在规范的SOP和严格的QA流程管理下,确保每个实验高标准完成。
